Tanıya yaklaşım çeşitleri
Genellikle hastalarımıza tanı koymaya çalışırken birbirini tamamlayan iki farklı yaklaşımı bir arada uygularız: [highlight color=”yellow”]İlki[/highlight] bir şablon ya da kalıbın tespit edildiği [highlight color=”blue”]“patern tanıma”[/highlight]yaklaşımıdır.[1-4] Erizipel ya da zona döküntüsünü görüp tanıma, fraktür, hareketsizlik ve nefes darlığı ile pulmoner emboli birlikteliği, batında şişlik, medusa başı, spider anjiyom mevcudiyetinde karaciğer sirozu tanısı gibi hekimlerin alışık olup sık gördükleri şablonlara uyan fizik muayene bulguları ile hikaye özelliklerinin birleştirilmesi yoluyla konulan tanıları belirler. [highlight color=”yellow”]İkinci tanısal yaklaşım[/highlight] ise basit bir şablonun konuyu açıklamakta yetersiz kaldığı ve hekimlerin daha analitik bir yolda ayırıcı tanıları irdeledikleri [highlight color=”blue”]“olasılık temelli tanısal muhakeme”[/highlight] diyebileceğimiz [highlight color=”blue”]“probabilistik yöntem”[/highlight]dir.[5-9] Bu yöntemde hikaye, fizik muayene ve bulgulara göre hekimler muhtemel birkaç tanı belirler, her birinin olasılığını değerlendirir, bu olasılıklara göre her bir tanıyı koyduracak ya dışlayacak testler isteyerek bazı tanıları dışlayıp bir tanesi üzerinde yoğunlaşmaya çalışırlar. İlk yöntem tıp mesleğinin incelikleri ve mesleki tecrübe ile yakından ilişkiliyken, ikinci yaklaşım hastalıkların anatomi ve patofizyolojisi ile klinik çalışmalardan elde edilen verilerin değerlendirilmesini ve uygulanan tanı testlerinin sınır ve yetkinliklerinin bilinmesini gerektirir.
Bu aşamada en uygun yaklaşım, belirli bir şablona uymayan belirti ve bulguları kümeler halinde sıralamak ve ayrı birer [highlight color=”blue”]“klinik problem”[/highlight] halinde sebep-sonuç ilişkilerini düşünmektir. Bu klinik problemler ayırıcı tanıyı yapmak üzere olasılıkların ayrı ayrı değerlendirileceği bir liste oluşturmaya yardımcı olur. Örneğin, batında şişlik, medusa başı ve spider anjiyom ile başvuran hastada klinik problem olarak [highlight color=”yellow”]“defans ve rebound vermeyen, akut batın hüviyetinde olmayan açıklığı yukarı batan matite ile giden karın şişliği”[/highlight] ayırıcı tanı açısından fikir verici bir sorun olarak listelenmelidir.
Klinik problemler listelendikten sonra bu klinik problemleri açıklayacak ayırıcı tanılar belirlenir ve bu tanıların her birine bir olasılık atfedilir. Bu kısım, gereksiz tetkik ve girişimleri azaltmak açısından çok önemlidir. Tüm ayırıcı tanılar için gerekli tüm testlerin aynı anda yapılması hem hastaya ihtiyaç olandan daha fazla sıkıntı yaşatır, hem maliyetlidir hem de gereksizdir. Bu sebeple ayırıcı tanılar kabaca 3 ana şekilde gruplandırılır:
[box type=”shadow” align=”aligncenter” class=”” width=””]
- en muhtemel olandan başlayarak ihtimallerine göre (olasılık temelli ayırıcı tanılar),
- tanı konamaz ya da tedavi edilemezse hayatı tehdit edici sonuçlarının ağırlığına göre (prognoz temelli ayırıcı tanılar), ve
- tedavisi kolay, yan etkisiz ve çabuk olmasına göre (pragmatik liste).[10]
[/box]
[box type=”note” align=”aligncenter” class=”” width=””][highlight color=”yellow”]Bir örnek üzerinden gidelim: [/highlight]78 yaşında hipertansiyon ile başvuran ancak 6 ay içinde 10 kilo kaybettiğini belirlediğiniz bir hasta düşünelim. Hastamızın hikayesinde eşini 6 ay önce kaybettiğini, iştahsızlığı olduğunu ve 40 paket-yıl sigara içme öyküsü olduğunu belirliyoruz. Ayırıcı tanılarımız bu bulgu ve belirtilere göre öncelikle depresyon, hemen ardından da neoplazi yönünde olacaktır. Bu konuda değerlendirmeler sonuç vermez ve bu tanılar ekarte edilirse ardından yeni ayırıcı tanılar ile malabzorpsiyon gibi daha nadir ve düşük ihtimalli tanılara doğru yönlenilir.[/box]
Olası tanı listesi şekillendikten sonra sıralama yapıp bu tanılara bir olasılık atfetmek işimizi kolaylaştıracaktır. Olası tanılarımızın olasılıkları toplamı 1 olacak şekilde büyükten küçüğe doğru yaptığımız bu liste sayesinde testlerimizi seçeceğiz. [10-12]
Hekimler her bir tanının olasılığını belirlerken birkaç farklı yönteme başvurabilirler. Bu yöntemlerden biri [highlight color=”blue”]“dolaylı ya da sezgisel yaklaşım”[/highlight] diyebileceğimiz, hekimin benzer hastalardaki tecrübesi yardımıyla koymuş olduğu tanıları irdelediği, bu geçmiş bilgilerden de kaba bir olasılık çıkardığı yaklaşımdır. Bu yaklaşım mükemmel değildir, yakın zamanda görülen ya da absürt sonuçlanan vakalar daha rahat hatırlanır ve yeni kanıtlar, çalışmalar ve verileri dikkate almaz. Dahası, bu yaklaşım sadece kendi tecrübelerimizi içerdiğinden ancak kendi bilgimiz dahilinde doğru olabilir. Yeterince benzer vaka görmemiş olmak, konu hakkındaki bilgimizin yetersizliği gibi konulardan etkilenir. Hekimin sezgileriyle şekillenen bu yaklaşımdaki her aşama bias (yanlılık) ve rastlantısal hataya açıktır. [10,13] Eski hocalarımız bu gerçekleri çok öncesinden görmüş olacak ki, büyük kliniklerde hastaların tanı ve tedavilerinin planlanması için [highlight color=”yellow”]“konsey sistemi”[/highlight]ni yerleştirmişlerdir. Cerrahpaşa, Çapa, Hacettepe, Ankara Üniversitesi gibi köklü kurumların ahşap ve tarih kokan amfilerinde genç hekimlerin eksiksiz hale getirmeye çalıştığı dosyalar ile konseye çıkarılan hastaların tanı ve tedavilerinin şekillendiği toplantılar veriye ulaşmanın hiç de kolay olmadığı internet öncesi dönemin bence en önemli kurumlarının başında gelmektedir.
[box type=”note” align=”” class=”” width=””]Her ne kadar tanıdan ziyade tedavi ile ilişkili olsa da konsept olarak buraya uygun bir anımı aktarmak istiyorum: 10 yıl kadar önce bir ACLS kursunda eğitim verirken benden hem yaşça hem de tıbbi tecrübe yılı olarak çok daha büyük bir kursiyer ambulans hekimimiz [highlight color=”yellow”]“kendi tecrübelerine göre”[/highlight] ambulans ve alanda entübasyonun uygun olmadığını belirterek yapmadığını söylemişti. Analitik bakış açısıyla, o yıllarda, bir ambulans hekimi tarafından uygulanan resüsitasyonda alanda da ambulansta da entübasyon olmazsa olmazlardan biri olarak kabul ediliyor ve öğretiliyordu. Dahası, kanıta dayalı tıbbi yeni öğrenen bir genç hekim olarak “tecrübelerime göre” denildiği zaman kulaklarımdan alev çıkmaktaydı. Elbette, birbirimizi ikna edemediğimizi rahatlıkla söyleyebilirim. Ancak, yıl 2016’ya geldiğinde alanda ve ambulansta entübasyondan ziyade göğüs basısının öne çıktığını görüyoruz. Dahası, havayolu açık tutup ventile edilebildiği sürece ambu-maske ile devam etmenin sağkalım üzerinde negatif etkisinin olmadığının, hatta, yeterince tecrübesi olmayan hekim ve sağlık personelinin alanda uyguladığı entübasyonun mortaliteyi arttırdığının gösterildiği verilere sahibiz. Her ne kadar tıbbi olmayan bireysel kaygılarla entübasyon işinin sorumluluğundan kaçmak için böyle bir söylemde bulunduğu önyargımı hâlâ yenemesem de bu anekdot aslında tecrübe ve gözleme de saygı duymam gerektiğini bana hâlâ hatırlatır. Bu hekim arkadaşımızın, yıllar sonra, erken invazif girişim sayesinde sekelsiz iyileştiği anterior MI’a bağlı kardiyak arestinin alanda ilk müdahalesi esnasında kendi meslektaşlarından biri tarafından entübe edildiğini de söylemeden geçemeyeceğim. Bu açıdan, biastan arındırmamızın mümkün olmadığı tecrübe ve sezgilerimizle şekillenen yaklaşımlarımızı biraz analitik verilerle desteklemek yani orta yolu bulmak en doğrusudur diyebiliriz.[/box]
Test öncesi olasılık (pre-test probability)
İnternet sonrası dönemin nimetlerinden faydalanarak tecrübe ve bilgiyi bir araya getirmenin en doğru yol olduğu konusunda hemfikir olduğumuza göre nasıl yapacağımızı biraz irdeleyelim: [highlight color=”blue”]Sezgisel yaklaşımın[/highlight] aksine [highlight color=”blue”]“tamamlayıcı yaklaşım”[/highlight] diyebileceğimiz yöntemle [highlight color=”yellow”]“test öncesi olasılıklarımızı”[/highlight] yayınlanmış verilerden yola çıkarak belirlemeye çalışırız. Uygun bir çalışmada aynı klinik problem tanısal değerlendirme ile incelenmiş ve belirlenen tanıların frekansları bildirilmiş ise bu verileri test öncesi olasılık olarak kullanmak son derece yerinde olacaktır. Bu açıdan gözlemsel kohort çalışmaların aslında ne kadar önemli veriler sağladığını bir kez daha görmüş oluyoruz. Kullanabileceğimiz bir başka uygun çalışma tipi de klinik karar verme kuralları oluşturan çalışmalardır. Bu çalışmaları yürütürken, araştırmacılar, belirli bir klinik probleme sahip hastaları (anoreksi ve kilo kaybı) tanısal değerlendirmeye tabii tuttuktan sonra hastaları hedef durum açısından (bir tanı, mesela malignite, ya da sonlanım, mesela mortalite) farklı tanısal olasılıklara sahip alt gruplara (düşük, orta, yüksek risk) bölmek için istatistiksel yöntemler uygularlar.
Test sonrası olasılık (post-test probability)
Klinik tanı dinamik bir süreçtir. Uygulanan testlerden yeni veriler geldikçe bazı tanıların olasılıkları azalırken diğerleri artar. [highlight color=”yellow”]Olabilirlik Oranları (Likelihood Ratio [LR])[/highlight] yeni verilerin tanısal olasılıkları ne derece değiştireceğini bize bildiren en önemli belirteçlerdir. Test öncesi olasılık, testin sonucuna göre bir test sonrası olasılığa dönüşür. Bu test sonrası olasılık testin pozitif olduğu durumda artarken, negatif olduğu durumda azalır. İşte, test öncesi olasılığın hangi test sonucuna göre ile hangi katsayıyla test sonrası olasılığa dönüştüğünü gösteren sayısal değer (katsayı) bu Olabilirlik Oranlarıdır.
Çoğu zaman hekimlerin tecrübe ile edindikleri sezgileri test sonuçlarının değerlendirmesinde gayet yeterlidir. Ancak bir test sonucunun, ayırıcı tanımızda yer alan bir tanı olasılığını arttırıp azalmasının ne derece güvenilir bir sonuç olduğu sistematik araştırma ve sayısal değerlendirme gerektirir. Bir hastada CRP’nin ya da Beyaz Küre Sayısının belirli bir eşiğin altında (negatif) olması ayırıcı tanılar içinde yer alan bakteriyel pnömoni ihtimalini elbette azaltır. Bu azalmanın anlamlı ve güvenilir olup olmadığı ancak test doğruluğunu gösteren çalışmalar ve bu çalışmaların sistematik derlemelerinin incelenmesiyle kesin olarak söylenebilir.
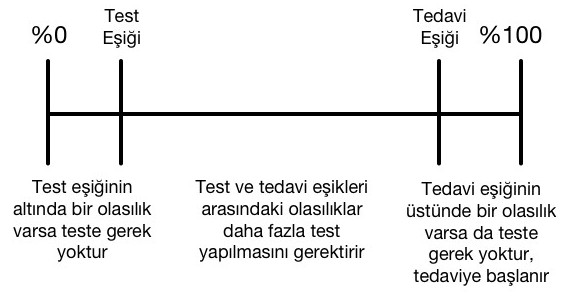
Tanısal süreçlerde test ve tedavi eşikleri
Bir tanının test öncesi olasılığı test eşiğinin altındaysa o tanı ihtimali test yapılmasını gerektirmeyecek kadar düşüktür. Eğer tedavi eşiğinin üstündeyse o zaman da test yapmaya gerek kalmaksızın tedaviye başlanmalıdır. Bir testin karar verme aşamalarında fayda sağlayabilmesi için teste endikasyon oluşturan tanı ihtimalinin test eşiğinin üstünde, ancak tedavi eşiğinin altında kalan bir oranda olması gerekir. Test sonuçlarının pozitif ya da negatif olmasına göre, o testin olabilirlik oranı (likelihood ratio) nispetinde testin konfirme ettiği tanının olasılığı da artar ya da azalır. Test sonrası olasılık, test öncesi olasılık ile test sonucunun olabilirlik oranının çarpımına eşittir. Test sonrası olasılık da tıpkı test öncesi olasılık gibi tedavi eşiğinin üstünde ise tedaviye başlanır, test eşiğinin altındaysa tanı ekarte edilmiş olur.[14,15] Bu eşiklerin izafi gösterimi aşağıdaki şekilde verilmiştir.
[box type=”shadow” align=”aligncenter” class=”” width=””]Bu aşama ve eşiklerin her zaman sayısal olarak hesaplanmasına gerek yoktur. Mesela, patern tanıma yoluyla tanı koyan tecrübeli bir hekim dermatom üzerinde klasik zona döküntülerini gördüğü anda sezgisel olarak test öncesi olasılığının çok yüksek, neredeyse %100’e yakın olduğuna kanaat getirerek tedaviye başlar. Aslında, test öncesi olasılığın tedavi eşiğinden yüksek olduğuna karar vermiştir. Benzer şekilde, aynı hasta yan ağrısı şikayeti ile başvurmuş olsa muayene yapmadan önce renal koliğin yüksek olasılıklı bir tanı olduğunu düşünecektir. Yani, yan ağrısı şikayeti olan bir hastada renal kolik test öncesi olasılığı yüksek olan bir tanıdır. Ama her biri ayrı birer test olan döküntülerin varlığı ve kostovertebral açı hassasiyetinin yokluğu bulguları sonucunda renal kolik için test sonrası olasılık, test eşiğinin altına düşer. Dolayısıyla da renal kolik tanısı koymak ya da ekarte etmek için herhangi bir test yapmaya gerek duymadan bu tanıyı ayırıcı tanı listesinden çıkarır. Keşke, hastalarımızdaki tüm tanıları bu kadar kolaylıkla doğrulayıp ekarte edebilseydik. Ama ne yazık ki, çoğu zaman sezgisel yaklaşımımız yetersiz kalır.[/box]
[highlight color=”yellow”]Peki, bu test ve tedavi eşiklerini nasıl seçiyoruz?[/highlight]
Bu eşikler testin gücü ve özellikleri, hastalığın prognozu ve tedavinin doğasından direk olarak etkilenir. Test ne kadar ucuz, kolay ve güvenilirse, tanının atlanması ne kadar tehlikeliyse, ve tanı konulursa verilecek tedavi ne kadar ulaşılabilir ve etkinse test eşiğimiz de o kadar düşer. Tersi durumlarda ise test eşiğimizi yüksek tutarız.
[box type=”shadow” align=”aligncenter” class=”” width=””]Örneğin, künt batın travması ile başvuran hastalarda serbest sıvı tespiti için tecrübeli ellerde FAST ile DPL’nin doğruluk, özgüllük ve duyarlılıklarının aynı olduğu gösterilmiştir. Bu sebeple de ATLS, ATACC, BTACC, NICE, KADAT gibi kurs ve kılavuzlar FAST bakısını DPL’nin önüne koymaya başlamıştır.
Peki, elimizde USG cihazı yoksa, FAST yapmaya karar verdiğimiz her hastaya DPL yapmaya da karar verir miydik? Büyük ihtimalle, intrabdominal kanama yönünden test öncesi olasılığımızı bir daha sorgular, ardışık vital ve fizik muayenelerle test öncesi ihtimalimizi düşürmeye ya da yükseltmeye çalışırdık. Elimizde USG varsa FAST için test eşiğimiz düşük, DPL için yüksektir. Bunun sebebi de girişimin invazifliğinden kaynaklanmaktadır.
Az önceki örnekte yer alan 35 yaşındaki karın ağrısı hastasında neredeyse tüm Acil Tıp hekimleri EKG isteyecektir. Çünkü EKG ucuz, non-invazif ve güvenilir bir testtir. Belki yılda 2 en fazla 3 kez görebileceği 35 yaş ve altı AKS’lerden birini yakalamak için tüm hastalara EKG çekilmesi bile anlamlı olabilir. EKG için her türlü ağrıda test eşiği çok ama çok düşüktür.
Yaşlı, immobil, malignite hikayesi olan, nefes darlığı ve yan ağrısı ile başvuran, akciğer filminde infiltrasyon görülmeyen bir hastada pulmoner emboli tanısı için BT anjiyogram test eşiği yüksektir, DMAH ile tedavi eşiği ise kontraendikasyon olmadığı sürece düşüktür. Kontrast nefropatisi ihtimali, hastanın BT’de görüntü verebilip veremeyeceği, yaşlı ve hipoksik bir hastanın gantri içinde monitörizasyonunun zorluğu gibi faktörler bizi hemen anjiyografi order etmekten geri tutarken, bir yandan da aslında test öncesi tanı olasılığımız çok yüksek olduğundan direk tedavi başlayıp başlamamak arasında kalırız. Aslında tedavi eşiğine oldukça yakın bir test öncesi olasılık söz konusudur. Aynı zamanda tedavi seçenekleri kısıtlı, alternatifleri dar ve kesin tedavisi olmayan bir tanı söz konusudur. PE olsa bile belki de sadece DMAH alabilecek olan bu hastada bu sebeple tedavi eşiği iyice düşer ve test eşiğine nerdeyse yaklaşır.
Tam tersine, bazı malignitelerde evreleme laparatomisi adı altında cerrahi, bir tedavi değil tanı testi olarak kullanılır. Malignitelerin tedavisi o kadar zorlu, pahalı, invazif ve komplikedir ki tedavi eşiğimiz neredeyse %100’e yakındır.[/box]
Sezgisel yaklaşımda hekimin çalıştığı ortam ve kliniğin de çok büyük önemi vardır:
[box type=”shadow” align=”aligncenter” class=”” width=””]Örneğin, karın ağrısı şikayeti ile acil servise başvuran 35 yaşında bir hastada Acil Tıp hekiminin aklında prognostik ve probabilistik ayırıcı tanı listeleri aynı anda oluşur. En olası ön tanılar indigesyon, gastroenterit, meteorizm şeklinde başlayıp akut apandisit ile devam etse de, Acil Tıp hekimi [highlight color=”yellow”]“akut MI ya da aritmi de olmasın”[/highlight] demek için eğitilmiştir. Bir Genel Cerrahi hekimi aynı hastada sezgisel olarak önce perforasyon, herni, akut apandisit gibi tanıları elemeye çalışır. Dermatoloji hekimi zona olmadığından emin olmak ister. Bu açıdan her hastada tanının ne olmasını istediğimizi değil ne olabileceğini gözden geçirmemiz, bununla ilgili uygun çalışmalardan olası tanıların frekanslarını değerlendirmemiz çok önemlidir.[/box]
Kaynaklar
- Eva KW. What every teacher needs to know about clinical reasoning. Med Educ 2005;39:98–106.
- Vijayasekaran D, Ramesh S. Teaching and Assessing Clinical Reasoning Skills. Indian Pediatr 2016;53:175.
- Schmidt HG, Norman GR, Boshuizen HP. A cognitive perspective on medical expertise: theory and implication. Acad Med 1990;65:611–21.
- Carlos WG, Kritek PA, Clay AS, Luks AM, Thomson CC. Teaching at the Bedside: Maximal Impact in Minimal Time. Ann Am Thorac Soc 2016;:AnnalsATS.201601–018AS.
- Rebitschek FG, Bocklisch F, Scholz A, Krems JF, Jahn G. Biased Processing of Ambiguous Symptoms Favors the Initially Leading Hypothesis in Sequential Diagnostic Reasoning. Exp Psychol 2015;62:287–305.
- Monteiro SD, Sherbino JD, Ilgen JS, Dore KL, Wood TJ, Young ME, et al. Disrupting diagnostic reasoning: do interruptions, instructions, and experience affect the diagnostic accuracy and response time of residents and emergency physicians? Acad Med 2015;90:511–7.
- Croskerry P. A universal model of diagnostic reasoning. Acad Med 2009;84:1022–8.
- Ilgen JS, Humbert AJ, Kuhn G, Hansen ML, Norman GR, Eva KW, et al. Assessing diagnostic reasoning: a consensus statement summarizing theory, practice, and future needs. Acad Emerg Med 2012;19:1454–61.
- Ilgen JS, Eva KW, Regehr G. What’s in a Label? Is Diagnosis the Start or the End of Clinical Reasoning? J Gen Intern Med Published Online First: 26 January 2016. doi:10.1007/s11606-016-3592-7
- Guyatt G. Users’ Guides to the Medical Literature: A Manual for Evidence-Based Clinical Practice, 3E. McGraw Hill Professional 2014.
- Felder S, Mayrhofer T. Medical Decision Making. Berlin, Heidelberg: Springer Science & Business Media 2011. doi:10.1007/978-3-642-18330-0
- Sox HC, Higgins MC, Owens DK. Medical Decision Making. Chichester, UK: John Wiley & Sons 2013. doi:10.1002/9781118341544
- Richardson W. Where do pretest probabilities come from? Evidence-Based Medicine 1999;4:68–9.
- Pauker S. The threshold approach to clinical decision making. New England Journal of Medicine 1980;302:1109–17.
- Gross R. Making Medical Decisions. ACP Press 1999.