Alüminyum fosfitin (AlP) veya genel olarak metal fosfitin neden olduğu fosfin zehirlenmesi, özellikle Hindistan’da en yaygın ölüm nedenlerinden biridir. Bu kimyasal formülasyon “pirinç tableti” adı altında satılmakta olup, ticari ve endüstriyel kullanım için oldukça etkili bir pestisit olarak bilinmektedir. Ayrıca Celphos, Fostox, Phostoxin, Phostek, Quick Phos, Fumitoxin, Fieldphos, Talunex ve Weevil-Cide gibi marka isimleri altında da satılmaktadır. Metal fosfitlerin yüksek ölümcüllüğü, suyla reaksiyonu sonucu açığa çıkan fosfin gazından (PH3) kaynaklanmaktadır. Ortaya çıkan gaz renksizdir ve spesifik bir sarımsak veya çürük balık kokusuna sahiptir. Hemen hemen tüm canlı organizmalar için öldürücü olmasına rağmen halen en yaygın kullanılan pestisitlerden biri olan AlP’nin en önemli özelliklerinden biri de kullanım kolaylığı ve ürünlerde kalıntı bırakmamasıdır. Tabletlerin havanın ve ortamın nemi ile reaksiyonu sonucu ölümcül fosfin gazı açığa çıkar ve ortamda yayılır. Bu tabletlerin kullanımında önemli olan fosfin gazının ortamdan uzaklaştırılması için yeterli sürenin ayrılmasıdır. Bu aşamadaki ihmal, kazara ciddi zehirlenmelere ve hatta ölüme yol açabilir.
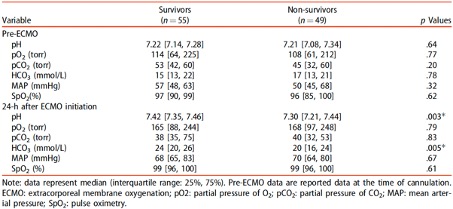
Alüminyum veya çinko fosfit, depolanan tahıldaki neme maruz kaldığında üretilen fosfin gazının solunması en yaygın maruz kalma biçimini temsil eder. Kasıtlı zehirlenme sonrası ölüm için risk faktörleri arasında doz (≥500 mg fosfit), hipotansiyon, asidoz, hipoksi, genel sol ventriküler hipokinezi ve sol ventriküler ejeksiyon fraksiyonunun <%40 olması yer alır. Şiddetli metalik fosfit zehirlenmesinin tedavisinden bağımsız olarak ilk gün içinde ölüm sıklıkla hızlı bir şekilde ortaya çıkar. Ölüm tipik olarak hücresel metabolizmanın bozulması sonucu kardiyak aritmilerden veya dirençli şoktan ve kalp yetmezliğinden kaynaklanır.
Fosfinin kusma, dışkı veya lavaj materyalinden gaz olarak salınabileceği ve sağlık hizmeti sağlayıcılarında ve maruz kalan diğer kişilerde solunum sıkıntısına neden olabileceği dikkate alınmalıdır. Bu nedenle bu hastalar negatif basınçlı odalarda tedavi edilmeli ve zehirlenen hastanın kusma ve dışkıları kapalı kaplara atılmalıdır.
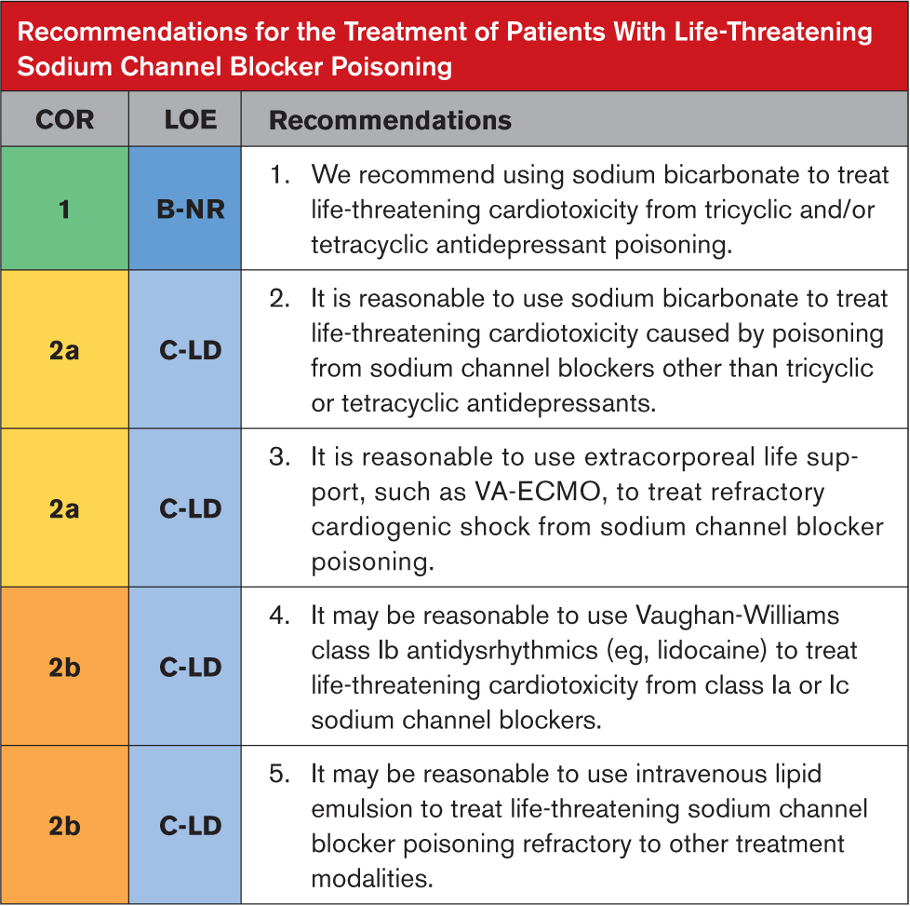
AlP zehirlenmesinin rutin tedavisi semptomatik tedavilerdir. Bunlar; ek oksijen, gerektiğinde endotrakeal uygulaması, hipovolemik şok düşünülen hastalarda izotonik salinle sıvı resüsitasyonu yapılması, hipoglisemi-hipokalemi-hipomagnezeminin tedavisidir. Öglisemik-insülin tedavisi faydalı olabilir. Mortalitenin azaltılmasında olan sodyum bikarbonat, magnezyum sülfat, trimetazidin, N-asetil sistein, C ve E vitamini, dihidroksiaseton, tiamin ve hidrokortizonun uygulanması etkili olabilir.
Vücutta fosfin gazı salınımı yoluyla, fosfinin solunum zincirini bozarak mitokondri düzeyindeki etkisine, sitokrom c fonksiyonunun engellenmesine ve hidroksil radikallerinin üretimine bağlı olarak hücresel solunum yetmezliği meydana gelir. Bugüne kadar bu zehirlenmeyi tedavi edecek kesin bir panzehir geliştirilmemiştir. Ancak ölüm oranını azaltmak için araştırmacılar tarafından çeşitli stratejiler uygulanmıştır. Hindistan cevizi yağının fosfin gazı emilimini hızla önlemede rol oynadığı; Dihidroksiaseton’un, mitokondri aktivitesinin sitokrom c’sini geri kazandırdığı gösterilmiştir. Kalp, AlP toksisitesinden etkilenen ana organlardan biridir. Melatoninin, kardiyotoksisiteyi hafifletmede, mitokondri aktivitelerini iyileştirmede ve oksidatif stres biyobelirteçlerini iyileştirmede etkili bir terapötik ajan olduğu gösterilmiştir. Bir antioksidan ve besin takviyesi olarak N-asetilsistein, hepatik nekrozu önleyerek AlP toksisitesinde etkili bir ajan olarak geliştirildi. N-asetilsistein tedavisinden sonra C vitamini verilmesi önerildi.
Bu çalışmada AlP kaynaklı toksisitenin tedavisi için Sevelamer (SVLM) uygulanması önerildi. SVLM ayrıca, kronik böbrek hastalığı veya son dönem böbrek hastalığı olan hastalarda hiperfosfateminin tedavisi için kullanılmaktadır. SVLM, iyon değişimi ve hidrojen bağlanması yoluyla fosfat gruplarıyla etkileşime girebilen amin ve amonyum içermeyen gruplara sahiptir. Fosfin gazının SVLM’deki amonyum gruplarıyla reaksiyona girebileceğini ve diğer organlara karşı yüksek reaktivitesini kaybeden ve dışkı yoluyla atılabilen fosfonyum tuzuna dönüşebileceğine dayanan in-vivo bir çalışmaydı. Bu çalışmada AlP dozu 40 mg/kg olarak belirlenmiş olup 70 kg’lık bir kişi için ALP’nin öldürücü dozunun 150 ila 500 mg arasında olduğu bildirilmektedir. Sıçanlar üzerinde yapılan bu çalışmada dört grup seçilmiş: 1.grup: kontrol grubu; 2. Grup: AlP ile zehirlenenler ve SVLM verilmeyenler; 3.grup 5mg/kg SVLM ile tedavi edilen AlP ile zehirlenenler; 4.grup: 10mg/kg SVLM ile tedavi edilen AlP ile zehirlenenler. Organ yaralanmalarının serum biyobelirteçleri, hayatta kalma yüzdesi kaydedilmiş olup serum biyobelirteçlerinin organ hasarı seviyesinin analizi ve adenozin trifosfat (ATP) miktarının ölçülmesi, SVLM’nin AlP zehirlenmesinde güçlü bir panzehir ajanı olarak görev yapabileceğini göstermişlerdir. Hayatta kalma yüzdesi, çalışmaların başlamasından itibaren art arda 7 gün içinde hesaplandı. Kontrol gruplarındaki hayvanların hepsi canlıydı. AlP ile zehirlenen hayvanlar ilk gün öldü. SVLM ile tedavi edilen iki grup zehirlenmiş hayvana ilacın iki dozu (yani 5 mg/kg ve 10 mg/kg) verildi. Yedi gün sonra 5 mg/kg SVLM ile tedavi edilen gruplarda hayatta kalma oranı %75 iken, daha yüksek dozda SVLM (10 mg/kg) ile tedavi edilen diğer grup, hayatta kalma yüzdesi 90 ile daha düşük bir ölüm oranıyla karşılaştı. Sonuç, SVLM’nin AlP zehirlenmesi için uygun bir tedavi olduğunu göstermektedir. Öte yandan, AlP verilen hayvanlar SVLM (5 ve 10 mg/kg) aldığında doku ATP içeriği daha yüksek seviyedeydi.
Tartışma
AlP veya pirinç tableti zehirlenmesi, yüksek ölüm oranıyla sonuçlanan en tehlikeli durumlardan biridir. Bu nedenle bu tür vakaların acil yönetimi hayati önem taşımaktadır. Yapılan bu çalışmada, SVLM’nin in vivo ölümcül AP dozuna karşı güçlü bir antidot etkisi olduğunu bulmuşlardır. AlP kaynaklı toksisitenin öldürücü dozun 40 mg/kg olduğu ve zehirlenen hayvanların tamamının ilk gün öldüğü gösterildi. İki doz SVLM (5 ve 10 mg/kg) tedavisi alan gruplar sırasıyla %75 ve %95 oranında hayatta kalmış. Ölümcül dozlarda (örn. 40 mg/kg) AlP’nin zehirlenmenin ilk saatlerinde hayvanların ölümüne neden olduğu bulunmuştur. Çalışmamızda da bildirildiği gibi bu doz sıçanlarda 24 saat içinde %70, 48 saat içinde %100 öldürücülüğe neden olmuştur. AlP’nin bu öldürücü dozu aynı zamanda organ hasarının sıçan serum biyobelirteçlerinde de önemli değişikliklere neden oldu. Verilerimiz, bu toksik maddenin yüksek ölümcül dozunda bile SLVM’nin ALP mortalitesinde önemli bir azalma olduğunu göstermektedir. Bu veriler SLVM’nin güçlü panzehir etkilerinden bahsetmektedir.
SVLM’nin AlP zehirlenmesine karşı panzehir rolü için çeşitli mekanizmalar sunulabilir. SVLM, polimerik yapıya sahip, hiperfosfatemi tedavisinde kullanılan bir hidrojel formülüdür. Amin hidroklorür içeren polimerler ve fosfat anyonları arasındaki bağlanma etkileşimi önceki araştırmalarda rapor edilmiştir. Bu bağlamda SVLM’nin in vitro fosfat iyonlarını önemli ölçüde yakalayabildiği rapor edilmiştir. SVLM yapısında klorür veya hidrojen karbonat iyonu ile karşılaşılarak hazırlanabilen amonyum tuzu mevcuttur. Fosfin zehirlenmesinin kontrolünde SVLM etki mekanizması için aşağıdaki etki yolu önerilmektedir. SVLM’de amonyum tuzu ve amin grupları bulunur. Fosfin gazının salınmasından sonra SVLM’nin uygulanması, diğer organlarda fosfin gazı dağılımını engelleyebilir. Fosfin, amonyum gruplarıyla reaksiyona girerek SVLM ile reaksiyona girebilir. Bu reaksiyonda iyonik tuz olan ve hidrojen bağlanmasıyla SVLM’nin polimerik ağında tutulabilen fosfonyum tuzu üretilir. Bu durumda, oldukça toksik olan zehir, toksisitesini kaybeden ve SVLM’nin polimerik ağında adsorbe edilen iyonik fosfonyum tuzuna dönüşür. SVLM klorür uygulanırsa fosfonyum klorür tuzu üretilecektir. Bu çalışmada sevelamer karbonat uygulandı. Bu uygulama için önerilebilecek diğer bir formül ise SVLM karbonattır. SVLM karbonatın etki mekanizması, SVLM için önerilen mekanizma ile aynı olabilir ürün ise fosfonyum karbonatın iyonik bir tuzudur.
Sonuç
SVLM, fosfatemi tedavisinde kullanılan bir nanotıp olarak kategorize edilir. Burada bu polimerik ilaç, AlP’nin neden olduğu toksisiteyi in vivo tedavi etmek için uygulanır. Sprague Dawley sıçanları arasında yapılan iki değerlendirmenin sonuçları rapor edildi. Mevcut çalışmada dört hayvan grubunun hayatta kalma yüzdesi kaydedildi. SVLM ile tedavi edilen AlP zehirlenmiş grupta düşük ölüm oranının gözlendiği tespit edildi. Organ hasarının serum belirteçlerinin analizi ayrıca SVLM’nin toksisiteyi ve organ hasarını azaltabildiğini gösterdi. Çeşitli organlardaki ATP seviyeleri, SVLM tedavisinin ATP tükenmesini önlediğini gösterdi. Ayrıca, AlP ile tedavi edilen hayvanlara kıyasla SVLM alan hayvanların farklı dokularında yüksek düzeyde ATP tespit edildi. SVLM etkisinin olası mekanizması, SVLM’de bulunan amonyum klorür veya amonyum karbonat gruplarıyla fosfin gazının zararsız ve SVLM ağında sıkışıp kalan fosfonyum tuzu üreterek reaksiyonudur.
KAYNAKÇA
1. Heidari R, Mohammadi HR, Goudarzi F, Farjadian F. Repurposing of sevelamer as a novel antidote against aluminum phosphide poisoning: An in vivo evaluation. Heliyon. 2023;9(4). doi:10.1016/J.HELIYON.2023.E15324
2. Overview of rodenticide poisoning – UpToDate. Accessed May 4, 2024. https://www.uptodate.com/contents/overview-of-rodenticide-poisoning?search=aluminum+phosphide&source=search_result&selectedTitle=1%7E5&usage_type=default&display_rank=1
3. Proudfoot AT. Aluminium and zinc phosphide poisoning. Clin Toxicol (Phila). 2009;47(2):89-100. doi:10.1080/15563650802520675