Doç Dr. İsmail Altıntop
Metamfetamin, genellikle beyaz renkli, acı tadı olan, toz veya hap olarak kullanılan uyarıcı bir ilaçtır. Kristal metamfetamin, cam parçaları gibi parlak, mavimsi beyaz kayalar gibi görünen, limon tuzunun görünümüne benzeyen kristal şekilli bir maddedir. Amfetamin ise dikkat eksikliği/hiperaktivite bozukluğunu [DEHB] ve uyku bozukluğu olan narkolepsi tedavisinde kullanılır. Bu yönden metamfetamin amfetamine benzerdir.
Metamfetamin, yüksek derecede lipofilik, santral sinir sistemi (SSS) üzerinde güçlü stimülan etkileri olan bir feniletilamin türevidir. Metamfetamin güçlü bir uyarıcıdır ve akut zehirlenme; kalp, beyin ve psikiyatrik belirtilerle hayatı tehdit edebilir. Uzun süreli kullanım ise kalıcı nörolojik ve kardiyovasküler hasar, bağımlılık ve ölüm riskini artırır. Son on yılda küresel çapta kullanım prevalansı artmış, özellikle “kristal met” formunun yaygınlaşmasıyla acil servislere başvuru ve mortalite oranlarında dramatik bir yükseliş gözlenmiştir.
İnsanlar metamfetamin nasıl kullanır?
- Sigara gibi içerek
- Yutarak (hap)
- Vaporizan aletler ile buharlaştırarak
- Su veya alkol içinde çözülmüş tozu enjekte etmek yoluyla alabilirler
Acil servislere gelen hastalarda sadece oral olarak kullanım değil, diğer kullanımlarda düşünülmelidir.
Metamfetamin etkisi “yükselme” olarak adlandırılan seviyeye çok hızlı bir şekilde ulaşır. İnsanlar genellikle “Aşırma veya daha fazla alma” olarak adlandırılan şekilde tekrarlanan dozlarda alma eğilimindedirler. Günde bir adet kullanan bağımlı yemeden uyumadan ilaç almaya meyilli hale gelebilir. Bu aşamada bağımlı, bir saat bile dayanamaz, her saat madde almaya devam eder. Bu durumun nedeni ilk aldığındaki yükselme hissi (Bulutlarda uçma, aşırı güven ve mutluluk) hissini elde etme arzusundan kaynaklanır. Neredeyse yemek tıkınır gibi, ardı ardına maddeyi almaya devam eder.
Metamfetamin beyni nasıl etkiler?
Metamfetamin beyindeki doğal dopamin miktarını artırır. Dopamin, vücut hareketi, motivasyon ve ödüllendirici davranışların güçlendirilmesinde rol oynayan ajandır. İlacın beynin ödül alanlarında yüksek düzeyde dopamini hızla salınım etkisi, uyuşturucu alma davranışını güçlü bir şekilde pekiştirerek kullanıcının deneyimi tekrar etme isteği uyandırır.
Fizyopatoloji ve Hücresel Toksisite
Metamfetaminin hücresel toksisitesi, monoamin salınımı, oksidatif stres, hipertermik kas hasarı kombinasyonuyla ortaya çıkar. Üç önemli etki mekanizması vardır. Bunlar;
1. Monoaminerjik Sistem ve VMAT‑2
Metamfetamin, presinaptik uçta dopamin (DA), norepinefrin (NE) ve serotonin (5‑HT) salınımını artırır ve geri alım taşıyıcılarını (DAT, NET, SERT) tersine çevirerek sinaptik aralıkta monoamin düzeyini yükseltir. Bu durum sempatomimetik fırtınaya ve nörotoksisiteye zemin hazırlar.
VMAT‑2 inhibisyonu, veziküllere DA alımını azaltır; sitoplazmik DA yükselir, bu DA’nın oto‑oksidasyonu ve MAO aracılı yıkımı artarak reaktif oksijen türleri (ROS) ve serbest radikal üretimini tetikler. Benzer mekanizmalar, monoamin metabolizmasında rol alan diğer durumlarda da oksidatif hasarla ilişkilendirilmiştir.
2. Sempatomimetik Fırtına ve Sistemik Toksisite
NE artışı; taşikardi, hipertansiyon, miyokardiyal oksijen tüketiminde artış ve yaygın vazokonstriksiyona yol açar. Bu; koroner vazospazm, iskemik kalp hastalığı, inme ve diğer iskemik komplikasyonların temel mekanizmasıdır.
Sempatik aşırı uyarılma, termoregülasyon merkezini de etkileyerek termoregülatuvar bozulmaya neden olur; benzer şekilde hipotalamik nöronların nöropeptiderjik dengesindeki değişikliklerin vazomotor belirtileri tetikleyebildiği gösterilmiştir.
3. Oksidatif Stres, Mitokondriyal Disfonksiyon ve Nörotoksisite
Yükselmiş sitoplazmik DA ve 5‑HT’nin oksidatif metabolizması, mitokondriyal geçirgenlik geçiş porunun (mPTP) açılmasını, membran potansiyelinin çökmesini ve sitokrom c salınımını tetikleyerek apoptotik/nekrotik hücre ölümüne yol açar.
ROS birikimi ve mPTP açılması, özellikle bazal ganglionlar ve striatumda dopaminerjik nöron kaybı ile ilişkilidir; benzer mekanizmalar diğer monoaminerjik bozukluklarda da nöronal sirkuit bozulması ve davranış değişiklikleriyle ilişkilendirilmiştir.
Hücresel Toksisite Mekanizmaları
| Mekanizma | Sonuç | İlişkili süreçler |
| VMAT‑2 inhibisyonu | Sitoplazmik DA ↑, ROS ↑ | DA oto‑oksidasyonu, MAO aktivitesi |
| mPTP açılması | Mitokondriyal depolarizasyon | Apoptoz/nekroz |
| Termoregülatuvar bozulma | Hipertermi, vazomotor instabilite | Hipotalamik nöron disfonksiyonu |
Figure 1 : Metamfetaminle ilişkili başlıca hücresel toksik yollar
Kısa Vadeli Etkiler
Küçük miktarlarda metamfetamin almak bile, diğer uyarıcılarla aynı etkilerinin çoğuna neden olabilir. Şunlardır;
-Uyanıklık ve aşırı fiziksel aktivite
-İştah azalır
-Solunum sayısı artar
-Kalp hızı artar veya düzensizleşir.
-Kan basıncı artar, vücut ısısı artar.
Uzun dönem etkileri
Metamfetamin enjekte eden kişilerde, HIV, hepatit B ve C gibi bulaşıcı hastalıklara yakalanma riski fazladır. Bu hastalıklar, uyuşturucu ekipmanında kalan kan veya diğer vücut sıvıları ile temas yoluyla bulaşır. Metamfetamin kullanımı, aynı zamanda enfeksiyon riskini artıran, korunmasız seks gibi riskli davranışlara yol açan muhakeme ve karar vermeyi de değiştiren bir maddedir. Ayrıca metamfetamin kullananlarda; bilişsel sorunlar, düşünme, anlama, öğrenme ve hatırlama ile ilgili sorunlar sık görülür.
Uzun süreli metamfetamin kullananalar da;
- Aşırı kilo kaybı
- Ciddi diş problemleri
- Deride yaralara yol açan yoğun kaşıntı
- Endişe ve anksiyete
- Beyin yapısı ve işlevindeki değişiklikler
- Bilinç bulanıklığı, konfüzyon
- Hafıza kaybı
- Uyku problemleri
- Şiddet içeren davranış
- Paranoya (başkalarına aşırı ve mantıksız güvensizlik)
- Halüsinasyonlar (olmasalar da gerçek gibi görünen duyumlar ve görüntüler)
Tüm bunlara ek olarak, sürekli metamfetamin kullanımı, beynin dopamin sisteminde, azalan koordinasyon ve bozulmuş sözlü öğrenme ile ilişkili değişikliklere neden olur. Uzun dönemde metamfetamin kullanan kişiler üzerinde yapılan çalışmalarda, beynin duygu ve bellekle ilgili alanlarını da etkilediği gösterilmiştir. Bu durum, metamfetamin kullananlarda görülen duygusal ve bilişsel sorunların çoğunu açıklayabilir.
Beyin değişikliklerinin bazıları, maddeyi bir yıl veya daha uzun süre bıraktıktan sonra geri dönebilse de, diğer değişiklikler uzun bir süre sonra bile düzelmeyebilir. Başka bir çalışma, bir zamanlar metamfetamin kullanan kişilerin ölüm riskinin arttığını göstermiştir. Parkinson hastalığının gelişmesi tetiklemektedir.
Bir kişi metamfetamin üzerinde aşırı doz alabilir mi?
Evet, kişi metamfetamini aşırı doz alabilir. Çok fazla madde kullandığında; ciddi, zararlı semptomlar veya ölümle sonuçlanan toksik reaksiyona neden olan aşırı doz alımı yaygındır. Tüm aşırı dozda uyuşturucu ölümlerinin yaklaşık yüzde 15’i metamfetamine bağlıdır. Bu ölümlerin yüzde 50’sinin aynı zamanda bir opioid madde içerdiği gösterilmiştir. Opioidlerden ise en fazla fentanil ile kullanılmaktadır. Sonuç olarak ucuz olarak elde edilen, sentetik opioidlerin bağımlılara madde temin eden kişiler tarafından bağımlının haberi olmadan sokak metamfetaminine eklendiğini düşündürmektedir.
İşte çoğu durumda maddeye fiziksel olarak bağımlı olan kişi bilmeden aldığı maddelerin farklı kombinasyonlarından dolayı ölümle karşı karşıya geldiği başka bir trajik durum yaşayabilir.
Metamfetamin doz aşımı nasıl tedavi edilebilir?
Metamfetamin doz aşımına bağlı sıklıkla inme, kalp krizi veya diğer organ sorunlarına yol açar. Klinik tablo, doz ve kullanım süresine bağlı olarak “hafif ajitasyon”dan “multiorgan yetmezliği”ne kadar uzanır.
| Sistem | Klinik Bulgular | Ekstrem Komplikasyonlar |
| Kardiyovasküler | Taşikardi, HT, Göğüs ağrısı | Miyokard Enfarktüsü, Aort Diseksiyonu |
| Nörolojik | Ajitasyon, Midriyazis, Psikoz | İntraserebral Hemoraji, Status Epileptikus |
| Termoregülasyon | Diyaforez, Ateş | Malign Hipertermi (>41°C) |
| Renal/Metabolik | Dehidratasyon | Rabdomiyoliz, Akut Tübüler Nekroz (ATN) |
Bu hücresel süreçler acilde gözlenen: ajitasyon/psikoz, hipertansif kriz, aritmi, hipertermi, nöbet, inme, rabdomiyoliz ve çoklu organ yetmezliği tablolarının biyolojik temelini oluşturur. Oksidatif stres ve mitokondriyal disfonksiyonun geri dönüşsüz nöronal hasara ilerlemesi, kronik kullanıcıda kognitif bozulma ve Parkinsonizm riskini artıran kalıcı hasara zemin hazırlar.
Metamfetamin toksisitesinde tedavi: Acil serviste temel yaklaşım
- İlk Yaklaşım ve Destek Tedavisi
ABC yaklaşımı:
Havayolu:
Şiddetli ajitasyon, bilinç değişikliği veya ciddi hipertermi varsa erken entübasyon.
Solunum: Yüksek akım O₂, solunum sayısı ve ETCO₂ takibi.
Dolaşım:
2 geniş damar yolu, EKG, kan basıncı, ritim monitörizasyonu, geniş spektrum tetkik (elektrolit, CK, böbrek fonksiyonu, troponin, laktat, kan gazı).
IV sıvı:
İzotonik kristaloid (0.9% NaCl veya Ringer laktat) ile hipovolemi, rabdomiyoliz ve böbrek hasarını önleme.
- Ajitasyon, Sempatomimetik Fırtına ve Psikoz Tedavisi
Birinci basamak: Yüksek doz titrasyonlu benzodiazepin
Midazolam IV/IM/IN veya diazepam/lorazepam IV.
Hedef: Ajitasyonun kontrolü, sempatik deşarjın ve dolayısıyla taşikardi/hipertansiyon ve hiperterminin azalması.
Yetersizse: Antipsikotik eklenebilir (haloperidol, olanzapin, droperidol; QT ve hipotansiyon takibiyle).
Fiziksel restriksiyon, yalnızca hayatı tehdit eden durumda, sedatifle kombine ve kısa süreli.
- Hipertermi ve Rabdomiyoliz Yönetimi
Giysi çıkarma, buharlaştırmalı soğutma, buz paketleri, soğuk IV sıvı.
Vakalarda 40 °C ve üzeri + kas rijiditesi varsa: Yüksek doz benzodiazepin, gerekirse nöromüsküler blokaj + entübasyon.
Parasetamol gibi antipiretikler etkisizdir.
Rabdomiyoliz:
Agresif IV sıvı; idrar çıkışı ≥1–2 mL/kg/s.
Hiperkalemi, asidoz ve AKI gelişirse nefroloji/diyaliz.
- Kardiyovasküler Komplikasyonlar
Hipertansiyon/taşikardi:
Önce sedasyon + sıvı.
Persistan hipertansif kriz için kısa etkili titrasyonlu vazodilatörler (örn. nitroprussid, nitrogliserin ± alfa‑bloker); saf beta‑blokerlerden (özellikle seçici) kaçınma eğilimi.
Göğüs ağrısı / iskemi: Standart AKS protokolü (ASA, nitrat, heparin, kardiyoloji).
Aritmiler: ACLS algoritmaları; özellikle K⁺, Mg²⁺, asidozun düzeltilmesi.
Özet Tablo: Acilde Ana Tedavi Hedefleri
| Klinik problem | Tedavi |
| Ajitasyon / psikoz | Yüksek doz benzodiazepin ± antipsikotik |
| Hipertansiyon / taşikardi | Sedasyon, sıvı, gerekirse vazodilatör |
| Hipertermi | Aktif soğutma, kas aktivitesini baskılama |
| Rabdomiyoliz / AKI | Agresif sıvı, elektrolit düzeltme |
Figure 1 Metamfetamin toksisitesinde başlıca tedavi hedefleri
- Nörolojik Komplikasyonlar
Nöbet: Benzodiazepin ilk basamak; devamında levetirasetam/fenitoin.
İnme şüphesi: Hızlı görüntüleme (BT ± BT anjiyo), nöroloji; reperfüzyon kararları standart inme protokollerine göre.
- Yatış, İzlem ve Uzun Dönem
Orta/ağır toksisite bulguları varsa (hipertermi, rabdomiyoliz, AKI, EKG değişikliği, nöbet, inme, ciddi psikoz) yatış.
Stabil, hafif olgular psikiyatri/madde bağımlılığı birimlerine yönlendirilerek taburcu edilebilir.
SONUÇ
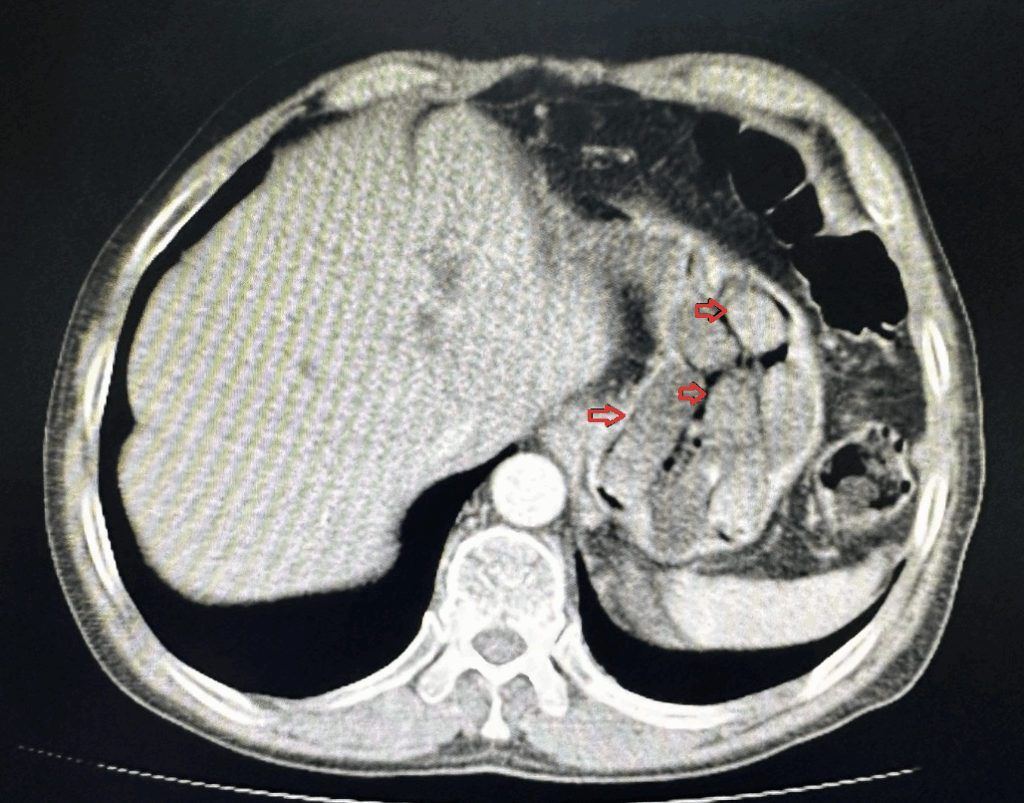
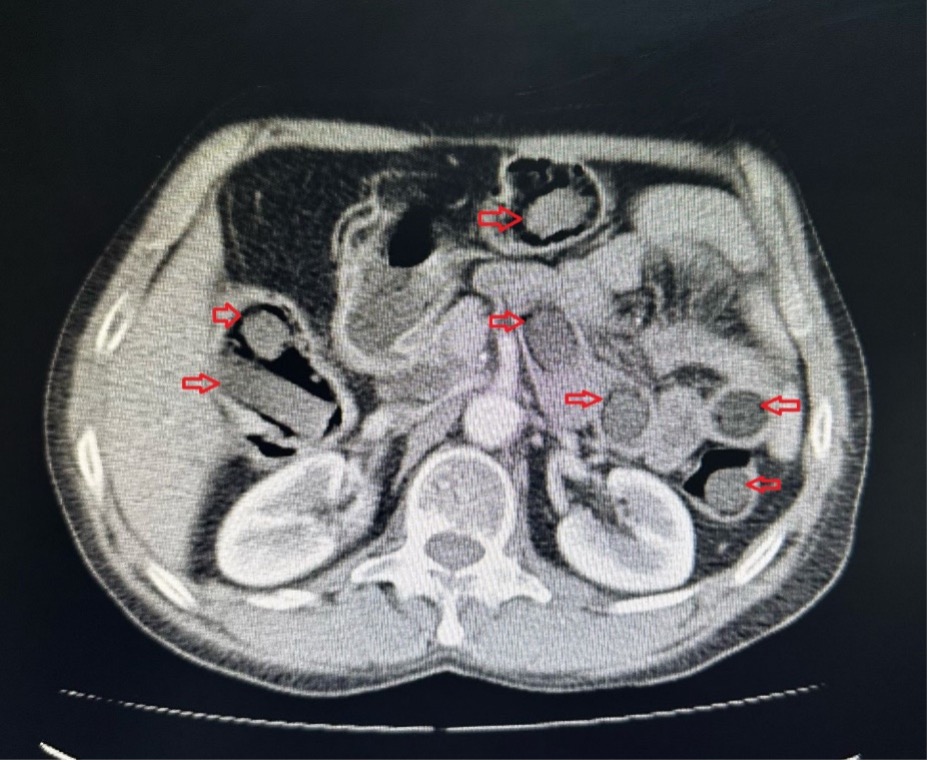
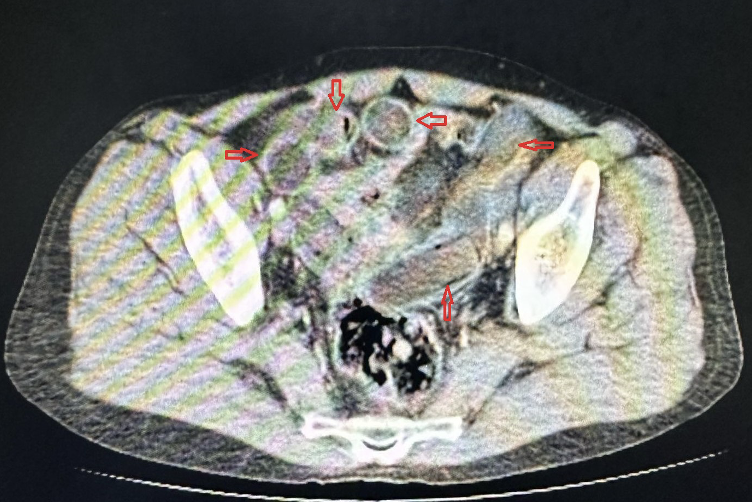
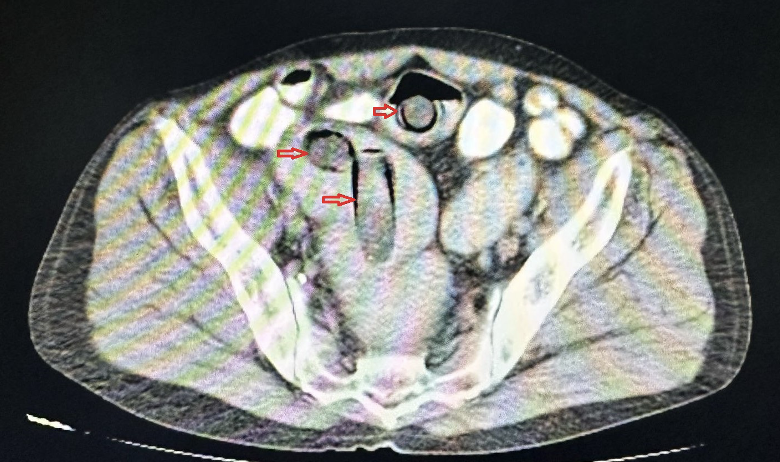
Metamfetamin (METH) zehirlenmesi, multisistemik tutulum gösteren ve acil tıp pratiğinde yönetimi zorlayıcı olan dinamik bir toksikolojik acildir. Yapılan güncel retrospektif çalışmalar, kanda metamfetamin saptanan vakalarda mortalitenin sıklıkla kardiyovasküler kollaps, yaygın visseral konjesyon ve kardiyak hipertrofi ile korele olduğunu ortaya koymaktadır. Klinik spektrumda, “plugging” olarak bilinen istemli rektal uygulama, yüksek mukozal vaskülarite ve emilim hızı nedeniyle intravenöz kullanımı taklit eden ani ve şiddetli sistemik toksisite tablolarına yol açabilmektedir. Ayrıca, karaciğer fonksiyonları normal seyretmesine ve hiperamonyemi görülmemesine rağmen gelişen METH ilişkili akut ensefalopati vakaları, ilacın kan-beyin bariyeri üzerindeki doğrudan nörotoksik etkisini ve tanısal süreçteki zorlukları kanıtlamaktadır. Klinik şüphenin düşük olduğu atipik semptomlu başvurularda dahi laboratuvar doğrulamasının yapılması, tanının netleştirilmesi ve uygun resüsitasyon stratejilerinin belirlenmesi açısından hayati bir araçtır.
Literatürdeki ekstrem vakalar ve polidrog kullanımı incelendiğinde, metamfetaminin alkol veya diğer uyarıcı maddelerle kombinasyonu, otopsi serilerinde saptanan mortalite oranlarını ve adli toksikolojik bulguların karmaşıklığını artırmaktadır. Özellikle kullanıcılar arasında, opioid ilişkili doz aşımı risklerini yönetmek amacıyla metamfetaminin bir “strateji” olarak kullanılması (örn. aşırı sedasyonu baskılamak için METH kullanımı), paradoksal olarak polidrog toksisitesini ve fatal seyreden kardiyorespiratuar olayları tetikleyebilmektedir. Paket sızıntısı kaynaklı “body stuffer” fenomeninde aniden gelişen dirençli status epileptikus ve 41°C üzerindeki malign hipertermi tabloları ise en yüksek mortalite riskini taşımaktadır. Bu bağlamda bildirilen vakalar, polisten kaçarken yutulan paketlerin gastrointestinal sistemde rüptüre olması sonucu gelişen masif intoksikasyonların, adli tıp ve acil tıp disiplinleri için en ölümcül senaryolardan biri olduğunu vurgulamaktadır. Bu durumlarda benzodiazepinlere ek olarak acil nöromüsküler blokaj, entübasyon ve agresif soğutma protokolleri zorunludur.
Klinik tabloyu ağırlaştıran diğer spektrumlar arasında; koroner risk faktörü olmayan gençlerde gelişen akut miyokard enfarktüsleri, bazal ganglion yerleşimli intraserebral hemorajiler ve gebelerde kontrolsüz vazokonstrüksiyona bağlı gelişen ablasyo plasenta yer almaktadır. Kronik maruziyette ise ejeksiyon fraksiyonunun %20’lere kadar gerilediği “Meth-heart” kardiyomiyopatisi, rabdomiyolize sekonder akut tübüler nekroz ve dopaminerjik nöron hasarı sonucu gelişen kalıcı parkinsonizm benzeri tablolar, bu zehirlenmenin kalıcı morbidite yükünü oluşturmaktadır.
‘’Metamfetaminin bağımlılık yapıcı etkisi oldukça yüksektir.’’
Metamfetamin almayan bağımlı; endişeli, tükenmiş bir görünüm, ağır depresyon, psikoz, yoğun uyuşturucu isteği olarak kendini gösterir.
Metamfetamin bağımlılığı nasıl tedavi edilir?
Metamfetamin bağımlılığını tedavi etmek için onaylanmış herhangi bir ilaç bulunmamaktadır. İyi haber şu ki, metamfetamin kötüye kullanımı önlenebilir ve ilaca bağımlılık davranışsal terapilerle tedavi edilebilir. Şimdiye kadar metamfetamin bağımlılığı için en etkili tedaviler, davranışsal terapilerdir.
Hastaların ilaç kullanımını tetikleyebilecek durumları tanımasına, bunlardan kaçınmasına ve bunlarla baş etmesine yardımcı olan bilişsel-davranışçı terapiler en etkili yöntemlerdir. Hastaları ilaçsız kalmaya teşvik etmek için ödüller kullanan motivasyonel teşvik terapileri başarılıdır.
İnsanlar, uzun süreli metamfetamin kullanımdan kaynaklanan çok sayıda tıbbi ve kişisel sorunu ele alan etkili tedavilere hazır ve istekli ise bağımlılıktan kurtulabilir.
KAYNAKLAR
- Naoi, M., Wu, Y., Maruyama, W., & Shamoto‐Nagai, M. (2025). Phytochemicals Modulate Biosynthesis and Function of Serotonin, Dopamine, and Norepinephrine for Treatment of Monoamine Neurotransmission-Related Psychiatric Diseases. International Journal of Molecular Sciences, 26. https://doi.org/10.3390/ijms26072916.
- Paulus, M., & Stewart, J. (2020). Neurobiology, Clinical Presentation, and Treatment of Methamphetamine Use Disorder: A Review.. JAMA psychiatry. https://doi.org/10.1001/jamapsychiatry.2020.0246.
- Tobolski, J., Sawyer, D., Song, S., & Afari, M. (2022). Cardiovascular disease associated with methamphetamine use: a review. Heart Failure Reviews, 27, 2059 – 2065. https://doi.org/10.1007/s10741-022-10261-7.
- Karakukcu, C., Ciraci, M. Z., Kocer, D., Zararsiz, G. E., Reyhancan, M., & Altintop, I. (2018). Regional drug abuse prevalence depending on laboratory based urine illicit drug screening results/Laboratuvar verilerine dayali idrarda yasa disi madde analiz sonuclarina gore bolgesel madde kullanim yayginliginin belirlenmesi. Anadolu Psikiyatri Dergisi, 19(2), 169-177.
- Nalçacı, S., Oruç, M., Şamdancı, E., & Güven, S. (2025). Otopsisi Yapılan ve Kanda Alkol, Uyutucu Uyuşturucu ve Uyarıcı Madde Tespit Edilen Vakaların Retrospektif Olarak İncelenmesi. Adli Tıp Dergisi, 39(2), 147-158.
- Ferrer, C. R., Muñiz, I. G., Guerrero, M. Á., Ferrando, J. P., Estean, M. Á. L., León, G. T., … & Martín, B. B. (2020). Amphetamine and methamphetamine poisonings attended in hospital emergency departments: clinical features and the usefulness of laboratory confirmation. Emergencias, 32, 26-32.
- Farag A, Nordt SP, Perese J. Methamphetamine Poisoning After “Plugging” Intentional Recreational Rectal Use. J Emerg Med. 2024 May;66(5):e597-e600. doi: 10.1016/j.jemermed.2024.01.004. Epub 2024 Jan 8. PMID: 38556372.
- Rabbany JM, Fitzgerald K, Bowman J, Dong F, Neeki MM. Methamphetamine-induced encephalopathy in the absence of hyperammonemia. BMC Psychiatry. 2023 Apr 20;23(1):276. doi: 10.1186/s12888-023-04764-2. PMID: 37081388; PMCID: PMC10120267.