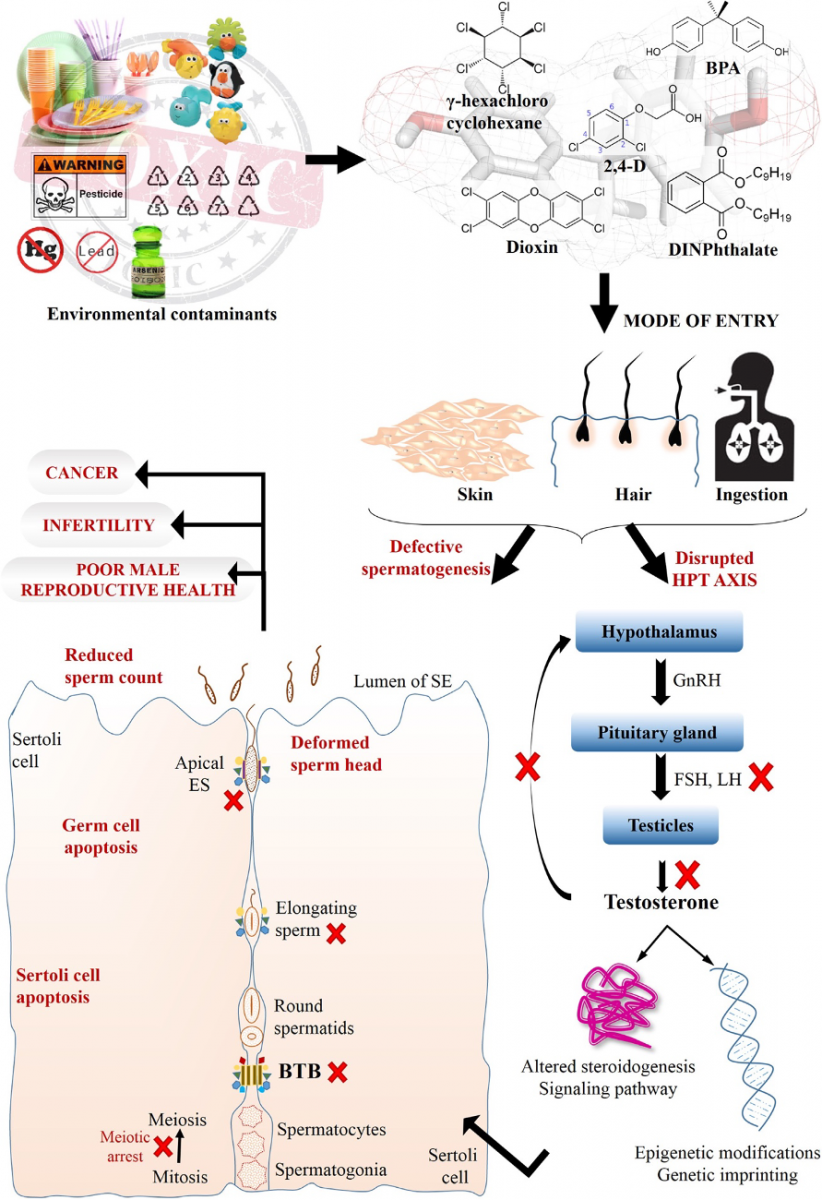
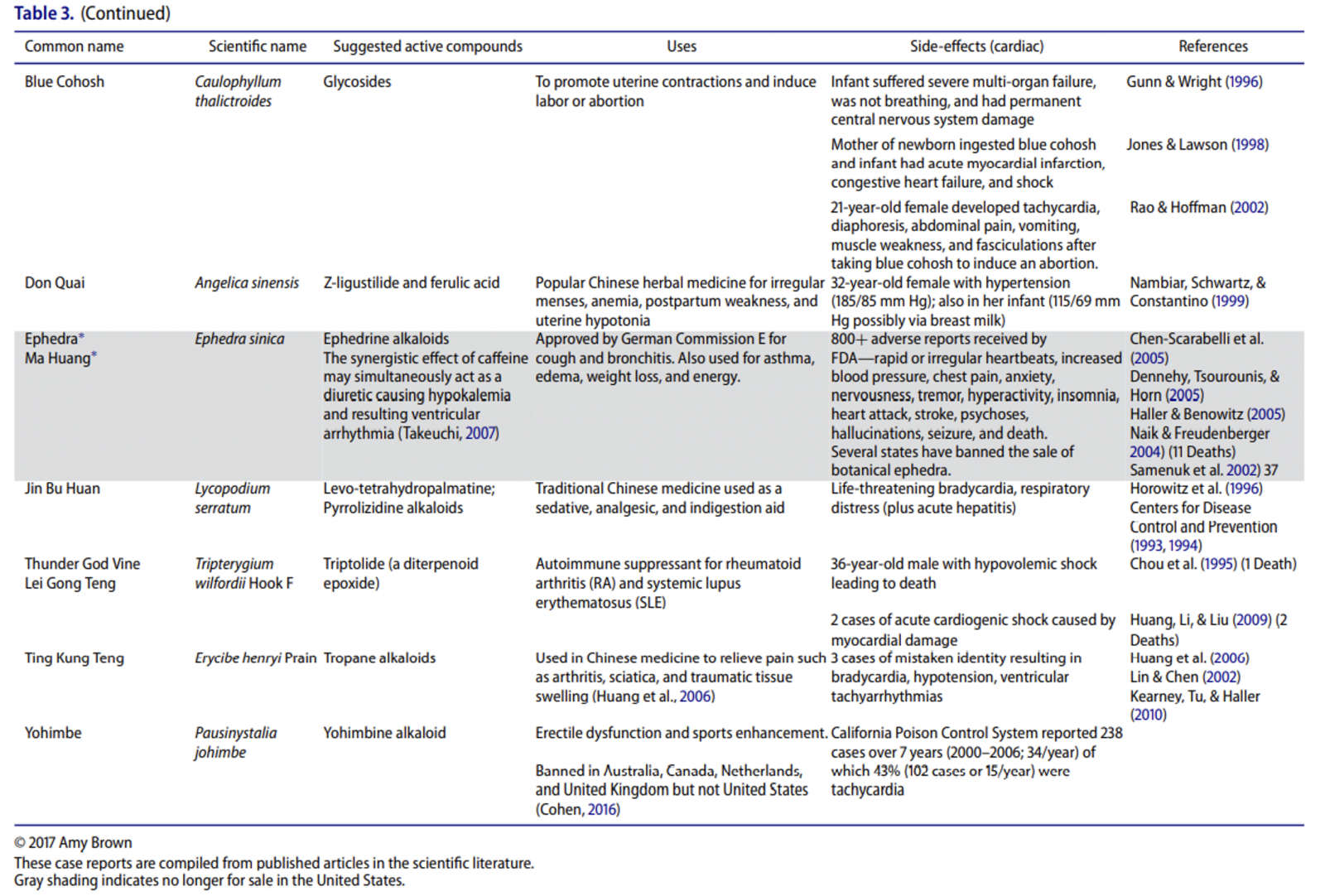
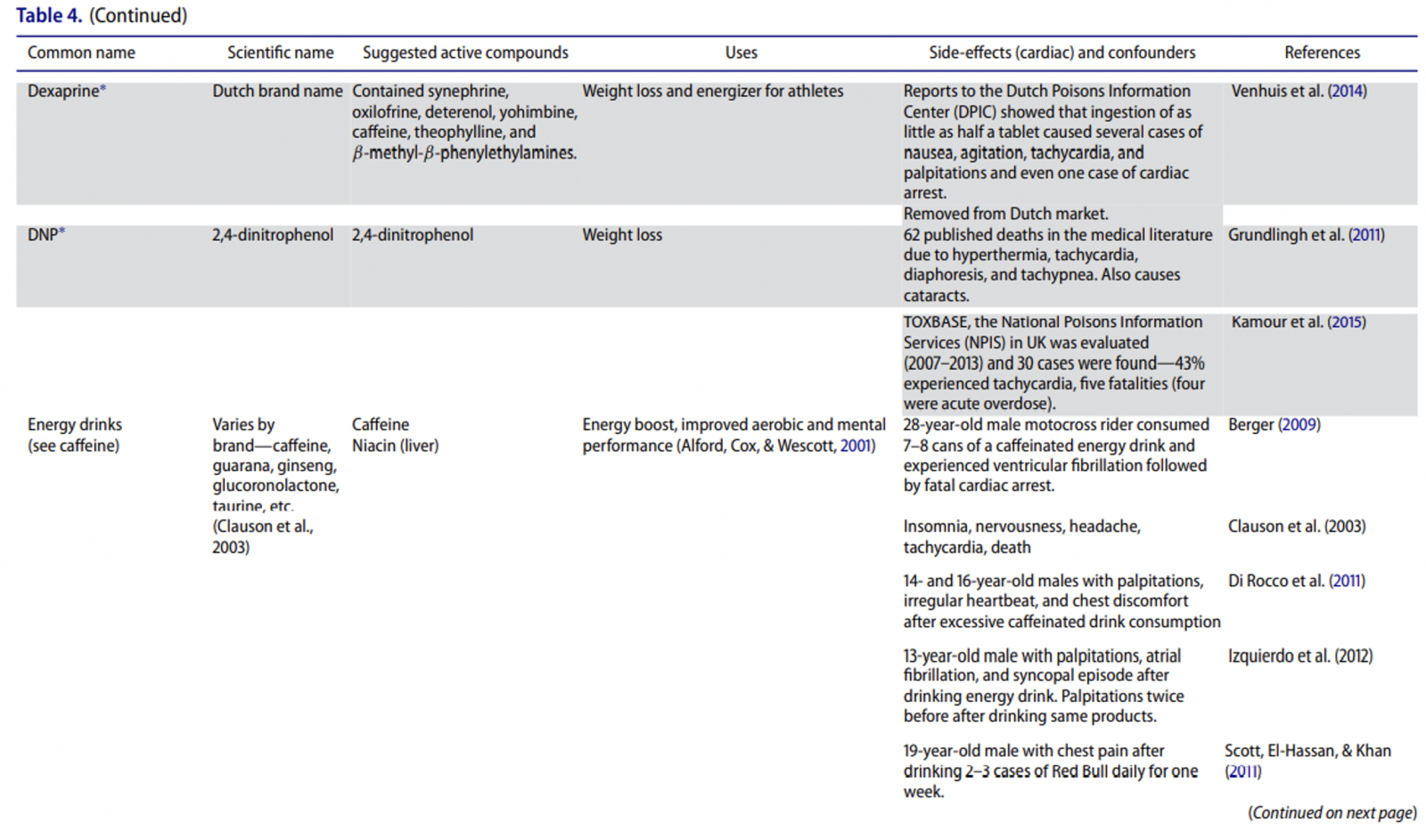
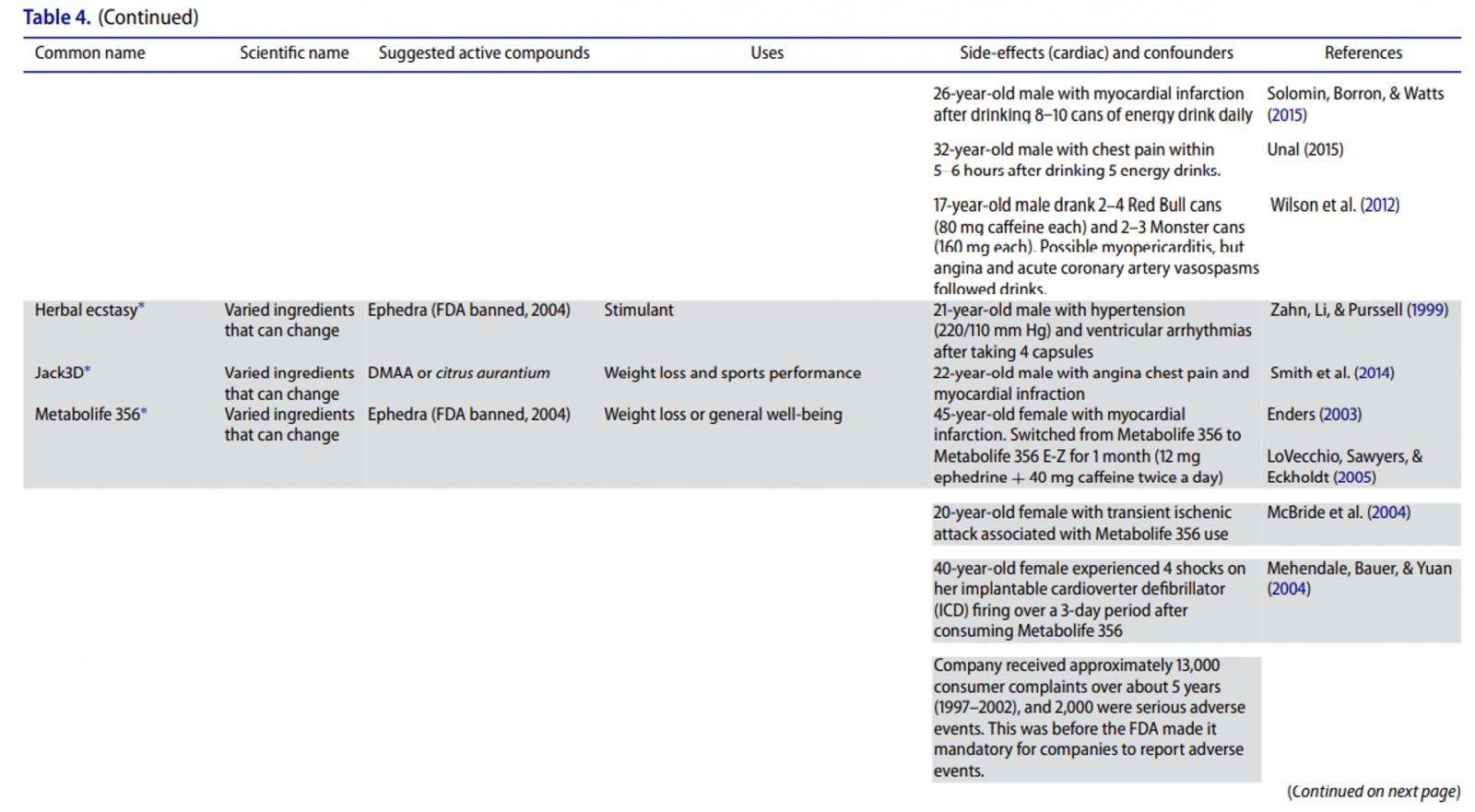
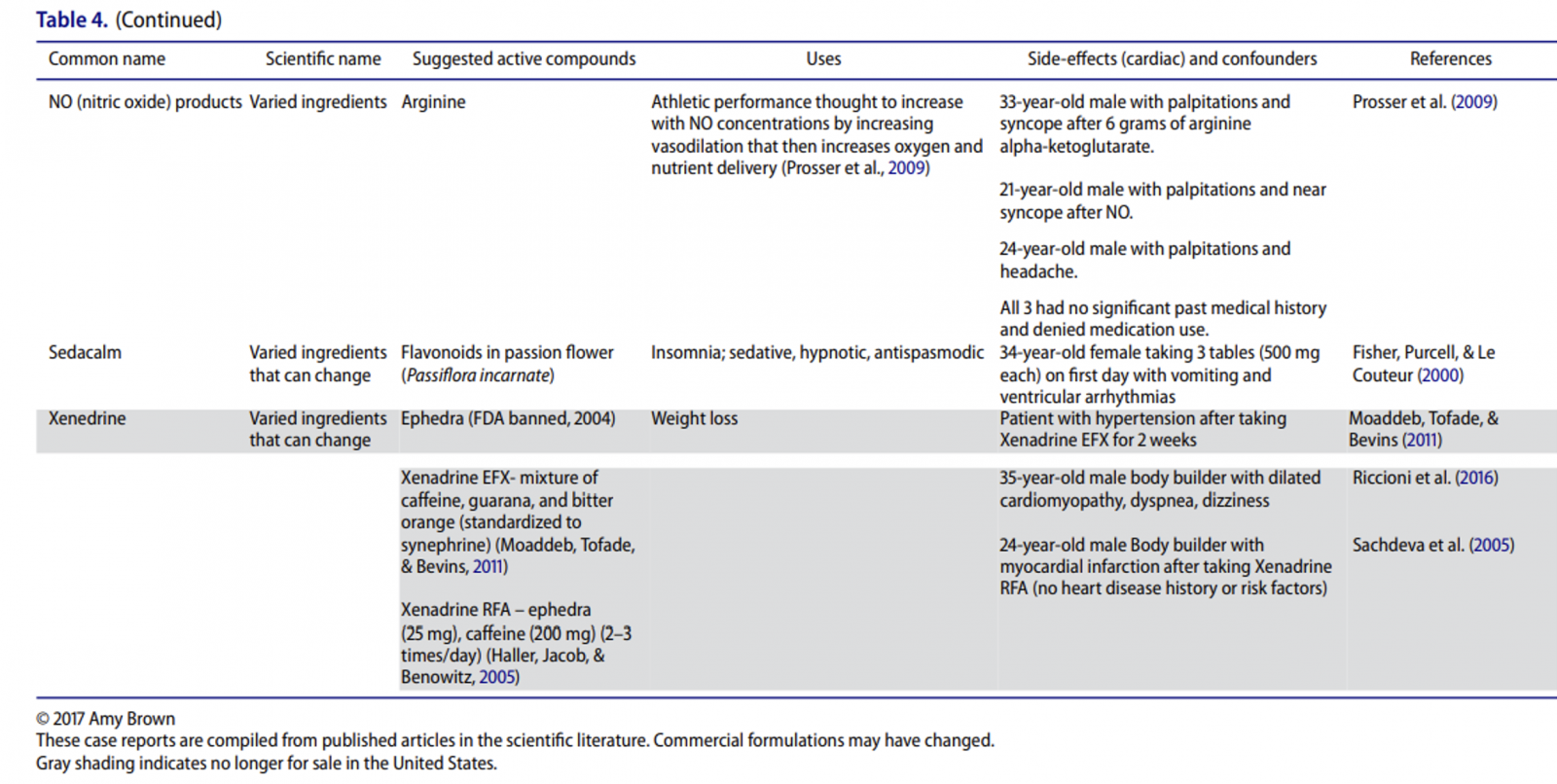
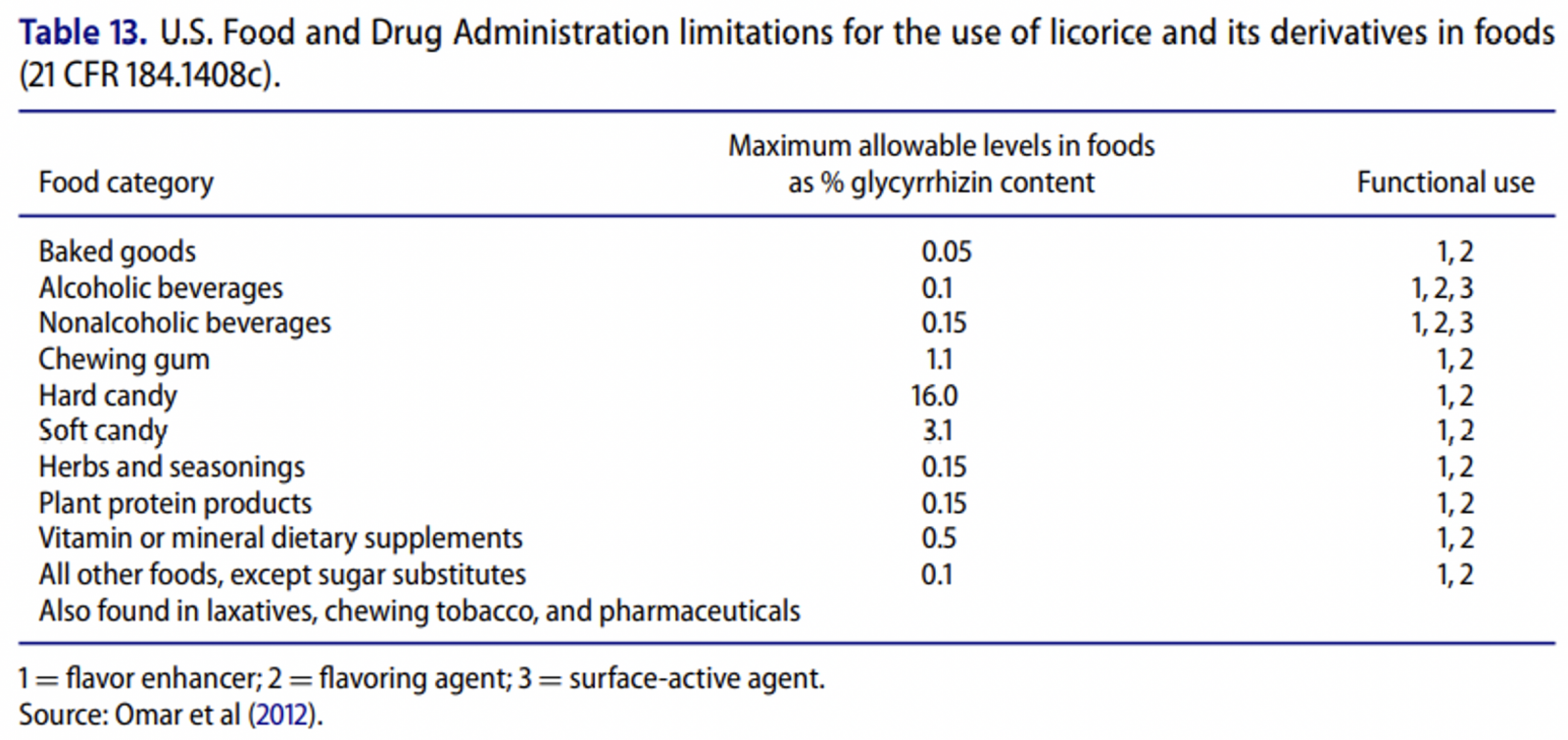
İnsanlık tarihinde yüzyıllardır şifalı bitki ve otlar çeşitli amaçlar için kullanılıyor. Günümüzde kullandığımız modern ilaçların büyük bir kısmı bitkisel kaynaklı. Her ilaç bir zehir potansiyeli de taşıdığı için şifalı diye adlandırılan, kullanılan bitkilerin toksik etkilerini de incelemek önem taşıyor. Bu yazıda “Cancer Related to Herbs and Dietary Supplements: Online Table of Case Reports. Part 5 of 5” 1 başlıklı makaleyi inceleyeceğiz. Başlıktan da anlaşılacağı üzere genelde otların kanserle ilişkileri derlenmiş ancak birçoğunun organlar üzerine toksik etkileri de mevcut. İyi Okumalar…
Giriş
Bu derleme aslında bir yazı dizisinin 5. Bölümü. İlk makalede besin takviyelerinin ve otların etkinliği, güvenilirliği incelenmiş arkasından karaciğer, böbrek ve kardiyak toksisite yapan ve kanser ilişkili olan 3 vaka bildirimi incelenmiş ve son olarak bu otlar ve besin takviyeleri bu yazıda tablo haline getirilmiş.
Tamamlayıcı ve alternatif tıbba olan ilgi her geçen gün artıyor ve günümüzde tamamlayıcı tıp da kendini akupunktur, besin takviyesi, ot, masaj, yoga, meditasyon, dua, enerji tıbbı, hipnoz vb araç ve yollarla tamamlıyor. Bu alanların kombinasyonlarına Hindistan’da Ayurvedic tıbbı, Japonya’da Kanpo veya Kampo, Çin’de Geleneksel Çin Tıbbı ismi veriliyor. Botanik bilimi tabi ki bu alanlarda çok önemli bir yere sahip çünkü günümüzde kullandığımız ilaçların %25-30’u bitkisel kaynaklı. Kanser konusunda ise bitkiler üzerinde yoğun araştırmalar mevcut. Amerikan Ulusal Kanser Ajansı ve Birleşik Devletler Ziraat Departmanı 15.000 bitkiden elde edilen 115.000 ekstreyi antikanser ajanı olarak test eden bir proje yürütüyorlar. Antiproliferatif özellik araştıran yüzlerce invitro çalışma halen devam etmekte. Bir çok botanik ürün güvenli olarak değerlendirilse de bir çok “doğal” ürün ise maalesef güvenilir değil.
Yöntem
Çalışma için PubMed’de, Ulusal Toksikoloji Programı (National Toxicology Program) , Dünya Kanser Araştırma Fonu (World Cancer Research Fund) ve Amerikan Kanser Araştırma Enstitüsü (American Institute of Cancer Research) veri tabanlarında “bitki ekstreleri”, “kanser”, “toksisite”, “ot”, “besin takviyesi” daha sonra bunlar “karsinojenik” anahtar kelimesiyle birleştirip seçilen vaka bildirimleri daraltılmaya çalışılmış. Eğer birden fazla bitkisel ürün karışımı varsa bunlar çalışmaya alınmamış. Mantarlar, zehirli olduğu bilinen bitkiler, suisid girişimleri, doz aşımları (vitamin/mineral harici), legal veya illegal madde kullanımları tabloya alınmamış.
Sonuçlar
1 Mayıs 2017 itibariyle PubMed’de; bitki ekstresi (152.425) , bitki ekstresi ve kanser (16.606), bitki esktresi ve kanser ve toksisiste (2.312), özet karşılarına çıkmış. Bu yöntemlerle bulunan otlar; aloevera, aristolochic asid, eğreltiotu, mavi devedikeni, öksürükotu, eşekkulağı, kanarya otu, Hint dutu, Kökboya bitkisi, Yerba Mate (Paraguay Çayı), Tesbih çiçeği, soya, sassafras ağacı. Son 50 yılda sadece 1 ot (guang fang ji- aristolochia kökü) üroepitelyal sarkom için, 2 besin (eğrelti otu ve sıcak mate çayı karsinojenik etkisiyle vaka bildirimleri bulunmuş.
Guang Fang Ji (Aristolochic asid ve içeren bitkiler)
Üriner sistem karsinomlarıyla ilişkili bulunmuş. Aynı zamanda Balkan Endemik Nefropatisine ( Bosna Hersek, Bulgaristan, Hırvatistan ve Sırbistan’daki çiftçilerde sık görülen bir nefropati türü) sebep olduğu; bu bölgedeki üroepitelyal kanserlerin sık görülmesinin tarlalarda aristolochic asid içeren bitkilerle olan temas olduğu düşünülüyormuş.
Balkanlardan ziyade Asya’da ve bir dönem Avrupa’da bu bitkilerin kullanıldığı bir çok bölge mevcut. 90larda Belçika’da bir diyet kliniğinin zayıflatmak için kullandığı otlardan biri buymuş ve bu hastaların %3-5’inde böbrek hasarı gelişmiş. 100’den fazla vaka bu grupta bildirilmiş. Vakaların 3’te 1’inin diyaliz ihtiyacı olmuş, 3’te 1’i böbrek nakline gitmiş kalan kısmı ise kronik böbrek hastası olarak kalmış. 2-6 yıl arasında ise bu vakaların %40-46’sında üroepitelyal karsinom gelişmiş.
Bu vakalardan sonra Geleneksel Çin Tıbbı uygulayıcıları Belçikalıların reçeteyi düzgün hazırlamadıkları için bu sonuç ortaya çıktığını söylese de, Tayvan üst üriner sistem kanserlerinin dünyada en çok görüldüğü ülke olarak biliniyor.
2001 yılından bu yana Aristolochic Asid ve içerikli ürünlerin ABD’ye girişi yasaklanmış ve dünyada bir çok ülke bu konuda Amerika’yı takip ediyor.
Hayvanlarda Kansere Sebep Olan Otlar
Bu makale insandaki kansere sebep olan maddeleri incelese de araştırma sırasında 9 bitkinin laboratuvar hayvanlarında kanserle ilişkili olduğu saptanmış.
- Aloe vera
- Öksürük otu
- Eşekkulağı
- Mabet bğacı
- Altın Mühür bitkisi
- Kanarya otu
- Kava bitkisi
- Kök boya
- Sasafras
Ek olarak 1 besin takviyesinin (Avlimil) farelere implante edilen insan meme kanseri hücrelerini stimüle ettiği bulunmuş. Bu yazı insan vaka bildirimlerini incelese de bu örnekler değerlendirilmeye alınmış çünkü potansiyel karsinojenlerin hepsi hayvan deneyleriyle belirleniyor.
Aloe Vera
İnsanlarda güneş yanığı ve yara iyileşmesinde uzun süredir kullanılan aloe vera yaprakları ve ekstresinin son zamanlarda içecekler ve takviye kapsül formları dahi mevcut. İnsanlarda yapılan çalışma yok ancak ratlarda oral yolla alındığında kolon adenoca ile ilişkili bulunmuş.
Öksürük Otu
Öksürük, bronşit, üst solunum yolu inflamasyonlarında sıklıkla kullanılan ot, ratlarda karaciğer hemanjioendotelyal sarkoma sebep olduğu bulunmuş.
Eşekkulağı
Almanlar eşekkulağı bitkisini yara-sıyrıklarda eksternal kullanımını onaylamış ancak Physician Desk Reference for Herbal Medicines (bir altenatif tıp kitabı) ratlarda karaciğer toksisitesi ve karaciğer kanserine sebep olabildiği için dikkatli olunması gerektiğini söylüyor. İnternetten satın alınabilen bir ot ancak FDA önermiyor; içeriğindeki pirolizidin alkaloidinin hayvanlarda hepatotoksik olduğu biliniyor.
Mabet Ağacı (Ginkgo Biloba)
Hafıza kaybı ve demans için kullanılan bu bitkinin yaprak ekstreleri yüzlerce yıldır Geleneksel Çin Tıbbında kullanılmasına rağmen insan çalışmaları henüz yeterli değil ve hayvanlarda ise karaciğer kanseri riskini artırdığı bulunmuş.
Altın Mühür Bitkisi (Goldenseal)
Amerikan yerliler gastrointestinal sistem enfeksiyonları, ishal ve cilt enfeksiyonları için kullanıyorlar. Rat çalışmaları karaciğer kanseri riskini artırdığını belirtmiş.
Kanarya otu
Kuzeybatı Amerika ve Meksika’da kolik ağrı ve epilepsi için kullanılıyor, hepatotoksik olduğu biliniyor.
Kava Bitkisi
Fare çalışmaları karaciğer kanseri riskini artırdığını belirlemiş
Kök boya (Rubia tinctorum L)
Kırmızı kök boya bitkisi renk verici olarak kullanılıyor, ratlarda hem böbrek hem de karaciğer kanseriyle ilişkilendirilmiş.
Sassafras
Kuzey Amerika ve Asya’da bulunan ağaçlarından elde edilen Safrole; bira ve çayda aroma verici olarak kullanılıyor. 60’larda laboratuvar hayvanlarında karaciğer kanseri ile ilişkilendirilmiş, aynı zamanda plasentayı geçtiği ve sütle de yenidoğana geçebildiği hayvanlar üzerinde tespit edilmiş. PubMed literatüründe çayının tüketilmesinden sonra insanlarda aşırı terleme vakası bildirilmiş. FDA’in, ABD’de kullanılmasını yasakladığı bir ürün daha.
İnsanlarda Kanserle İlişkili Besinler
Araştırmacılar ABD’deki kansere bağlı ölümlerin 3’te 1’inin diyet düzenlemesi yaparak önlenebileceğini öngörüyorlar. Bazı diyet parametreleri, besinler bazı kanserlerin oranını azaltıyor veya artırıyor (Tablo 5).
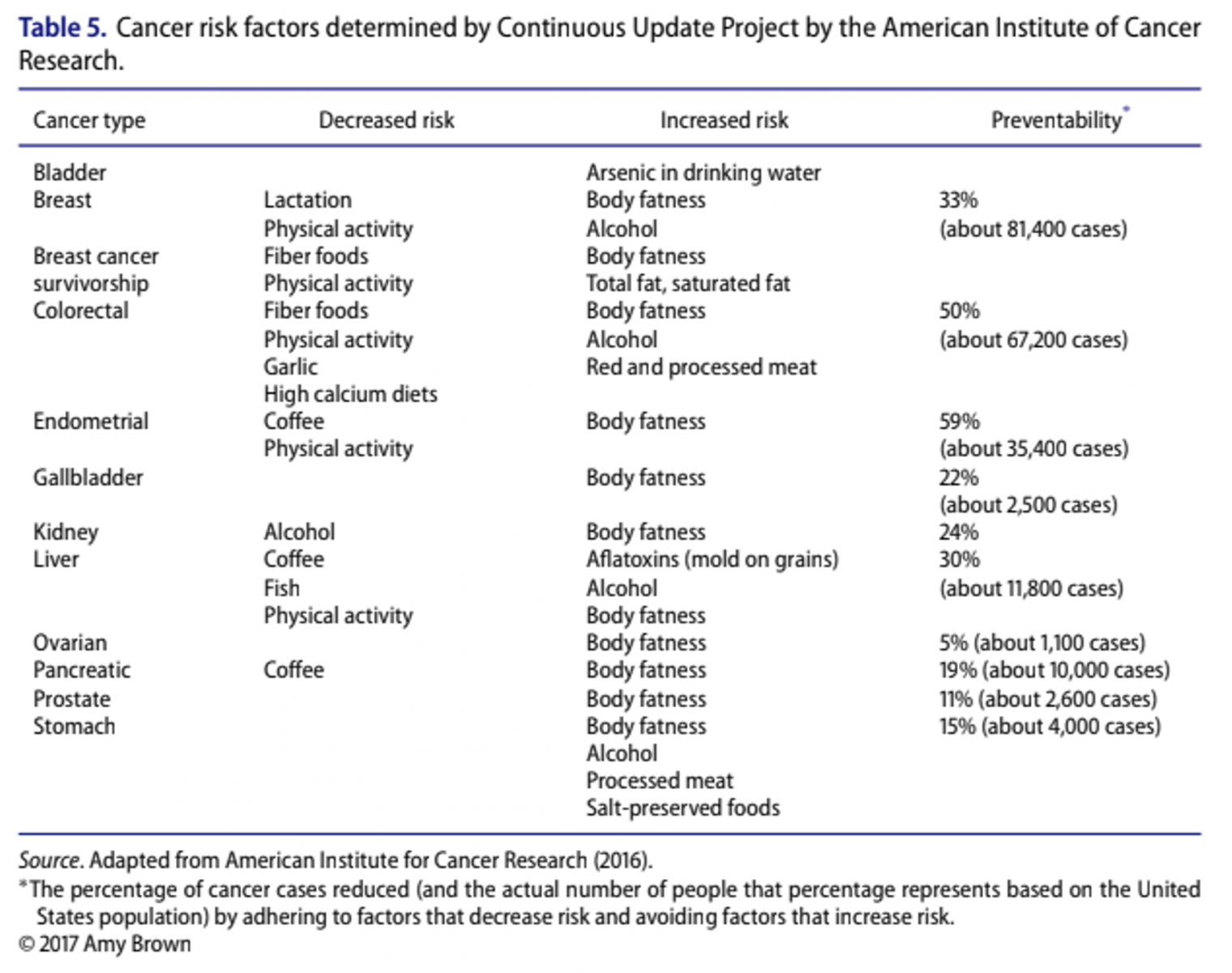
Ulusal Kanser Araştırma Ajansı (IARC) 45 yılı aşkın süredir bu konu üzeirnde çalışmalar yapıyor ve 1000’den fazla neden tanımlanmış durumda. Bunların arasında gün ışığı, tütün, ilaç, hormonlar, alkol, parazitler, mantarlar, bakteriler, virüsler, talaş, tuzlanmış balık, bazı otlar vb.
Amerikan Kanser Araştırma Enstitüsü (AIRC) ve Dünya Kanser Araştırma Fonu (WCRF) ise obezite, sedanter yaşam şekli, kırmızı ve işlenmiş etin fazla tüketimi, azalmış meyve sebze tüketimi, yetersiz anne sütü alımını kanser ilişkili olarak tanımlamış.
Eğreltiotu
Dünyada bir çok ülkede yetişiyor ve bir çok kişi kullanıyor.Mesane ve intestinal kanserlerle ilişkili kendisine FDA veri tabanında zehirli bitki olarak yer edinmiş.
Sıcak Maté
Çaya benzeyen Güney Amerikada yaygın olarak tüketilen kafein bazlı içecek.Brezilya ve Uruguay bölgesinde oral-özefagial kanserlerle ilişkilendirilmiş.
Soya Besinleri ve Genistein
Yapılan 2 farklı metaanalizde soya alımının meme kanseri rekürrensiyle ilişkili olmayıp, bazı vakalarda riski azalttığı belirlenmiş ve tamoksifen ve anastrozole tedavisinde çalışmalar sürmekteymiş (Chi et al., 2013; Magee & Rowland,
2012). Genistein ise bir antioksidan olarak bilinmekte ancak yapılan çalışmalardan hala anlamlı veri elde edilememiş.
İlaç Etkileşimleri
Doktorlar ve hastalar besin takviyelerinin tedavilerle çakışabileceğinin farkında olmalılar. Her zaman olduğu gibi; daha fazla bilgi sahibi olana kadar; karaciğer, böbrek, kalp, kanser hastaları, organ nakli olanlar, gebeler, emzirenler, başka ilaç kullananlar takviye besin veya bitkileri doktorları önermedikçe kullanmamalıdırlar.
Kısıtlılıklar
Çalışma ağırlıklı olarak PubMed ile sınırlı kalmış ve tüm literatürü göstermemekte. Dolayısıyla bitkilerin daha sık kullanıldığı Çin, Hindistan, Japon kaynaklarından bilgi yok sayılıyor. Bitki isimleri bölgeden bölgeye farklılıklar gösterebiliyor. Dolayısıyla burada olanlar ABD’de tanımlananlarla sınırlı. Bir diğer kısıtlama ise küflerin çalışmaya alınmamış olması. Çünkü küfler de besinler üzerinde bulunabiliyor ve potansiyel olarak karsinojenik olabilirler.
Kaynak
- Amy C. Brown (2018) Cancer Related to Herbs and Dietary Supplements: Online Table of Case Reports. Part 5 of 5, Journal of Dietary Supplements, 15:4, 556-581, DOI: 10.1080/19390211.2017.1355865